Anvisa pode liberar hoje Coronavac para crianças a partir de 3 anos
Caso aprovada pela agência, a vacina poderá ser utilizada imediatamente em todo o país em crianças e adolescentes
Publicado em: 20/01/2022 às 10:34 | Atualizado em: 20/01/2022 às 13:43
A Agência Nacional de Vigilância Sanitária (Anvisa) avalia, nesta quinta-feira (20), o uso emergencial da vacina Coronavac contra a covid-19 em crianças e adolescentes de 3 a 17 anos de idade.
A análise ocorre em reunião extraordinária da Diretoria Colegiada do órgão.
No entanto, para que o uso do imunizante seja aprovado, é necessário ter maioria favorável à utilização do fármaco.
Antes da votação, o diretor da Gerência Geral de Medicamentos, Gustavo Mendes, sugeriu que a vacina seja aplicada em crianças saudáveis, de 6 a 17 anos, e não de 3 a 17 anos, como solicitado pelo Instituto Butantan, fabricante da vacina.
A sugestão foi feita porque não há dados suficientes sobre a vacinação de crianças de 3 a 5 anos e imunocomprometidas.
A vacina já é aplicada na população pediátrica no Chile. Pesquisadores do país apresentaram dados sobre a imunização à Anvisa, mas não há evidências suficientes para o público mais jovem.
“Caso a diretoria decida pela aprovação da vacina, considerando as limitações, a nossa orientação é que a faixa etária seja limitada a crianças de 6 a 17 anos não imunocomprometidas. São os dados que nós temos com maior informação e sugestão de desempenho. Isso é corroborado pelas sociedades médicas”, pontuou Mendes.
A relatora do processo na Anvisa é Meiruze Sousa Freitas, da 2ª diretoria. Além da gestora, outros quatro diretores da agência devem formalizar voto: Antonio Barra Torres, Cristiane Rose Jourdan Gomes, Romison Rodrigues Mota e Alex Machado Campos.
Antes da deliberação, a Anvisa realizou uma série de reuniões com o Instituto Butantan, pesquisadores e sociedades médicas para avaliar os estudos clínicos sobre o uso do imunizante.
Leia mais no Metrópoles.
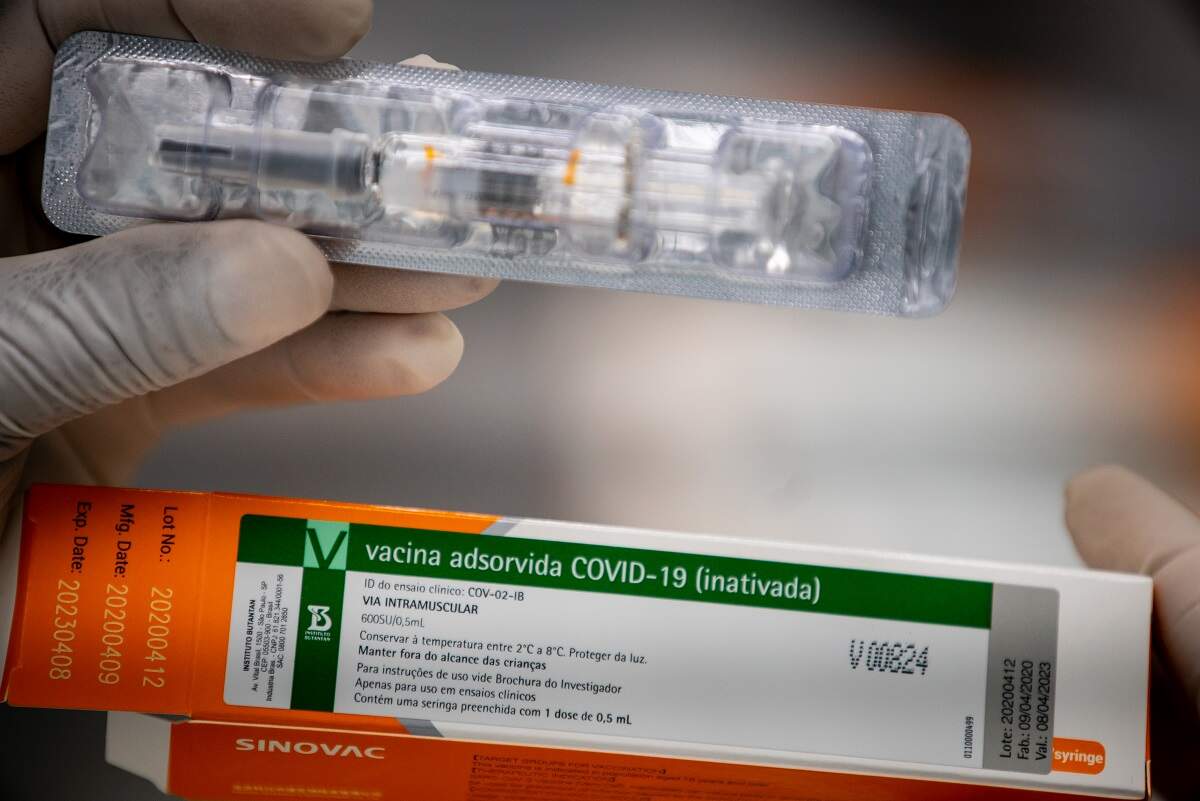
Foto: Divulgação
