Vacina chinesa coronavac pede aprovação à Anvisa
Instituto Butantan e Sinovac Biotech se organizaram para entregar documentação simultaneamente a agências do Brasil e China
Publicado em: 23/12/2020 às 14:02 | Atualizado em: 23/12/2020 às 14:04
O Instituto Butantan e o laboratório chinês Sinovac Biotech devem formalizar nesta quarta-feira (23) o primeiro pedido de registro da vacina coronavac, contra o coronavírus (covid-19), no Brasil.
A documentação final será entregue à Agência Nacional de Vigilância Sanitária (Anvisa) e também ao órgão regulador da China.
Dessa maneira, no Brasil, a coronavac será submetida a dois processos: registro sanitário — via normal para autorização de um medicamento, que permite aplicação de forma mais abrangente; e e autorização de uso emergencial — modalidade que permite liberação da vacina para grupos selecionados somente durante a pandemia.
Leia mais
Vacina do coronavírus já tem data para distribuição aos estados
Esta última, portanto, tem o prazo de dez dias para ter uma resposta da Anvisa. No entanto, o registro sanitário é mais demorado.
De acordo com o estudo, também devem ser conhecidos hoje as conclusões da fase 3 dos testes clínicos da coronavac.
Os ensaios foram realizados com cerca de 11 mil voluntários brasileiros da área da saúde.
Antecipação
Na segunda (21), a Anvisa antecipou a publicação do certificado de Boas Práticas de Fabricação da Sinovac.
Conforme a agência, este é um dos pré-requisitos para a liberação de uma vacina.
O Butantan prevê ter um total de 10,8 milhões de doses em solo brasileiro até o dia 31 de dezembro.
Já o governo de São Paulo mantém a previsão de começar a vacinar em 25 de janeiro, dependendo da decisão da Anvisa.
O Ministério da Saúde, após um recuo, decidiu pela compra da coronavac para uso no Programa Nacional de Imunizações (PNI).
Leia mais no Portal R7.
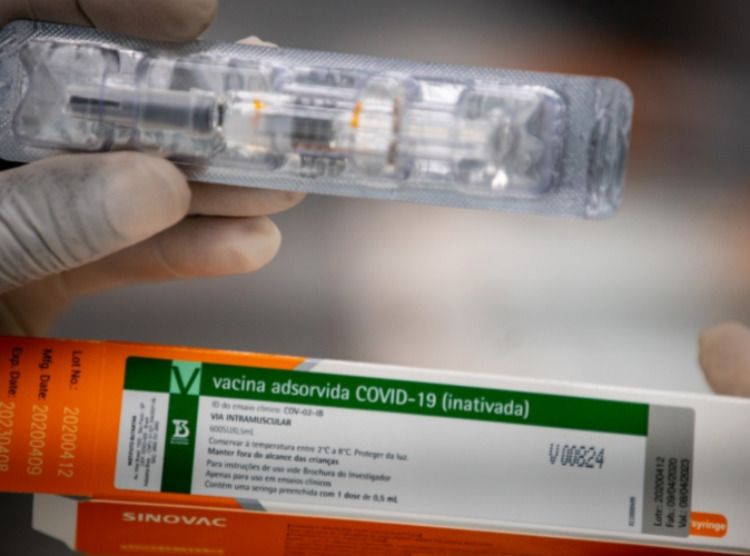
Foto: Divulgação/Instituto Butantan
